抗菌効果と安全性データ
目次
評価データ
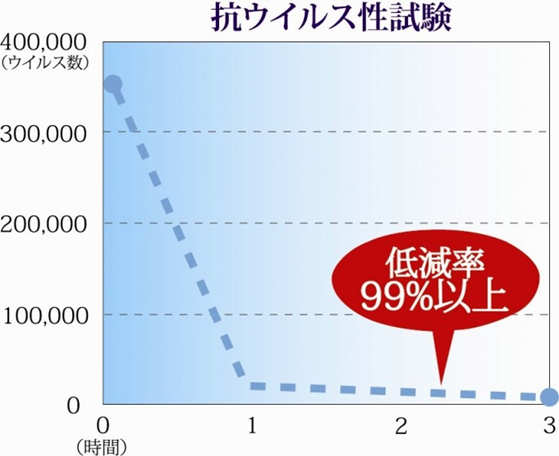
抗ウイルス性試験
- 評価機関
- NPO法人バイオメディカルサイエンス研究会
- 試験方法
- 新型インフルエンザ(H1N1Pdm)
A/California/07/09を使用しMDCK(イヌ肝臓細胞)を用いたプラーク法にて感染価を測定
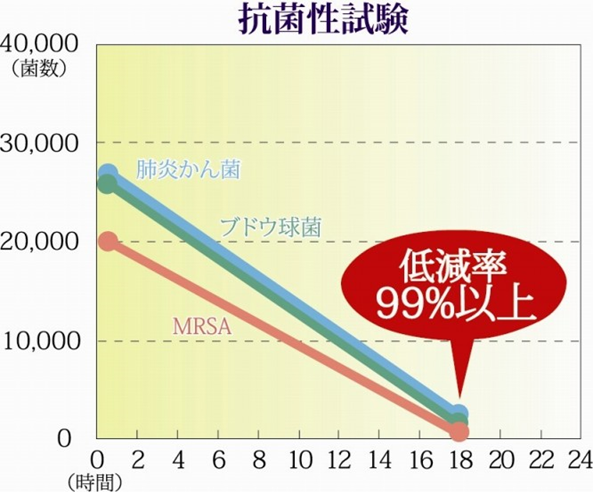
抗菌性試験
- 評価機関
- 一般財団法人 ボーケン品質評価機構
- 試験方法
- JIS L 1902
- 供試菌
- 黄色ブドウ球菌、肺炎かん菌、MRSA
防臭性試験
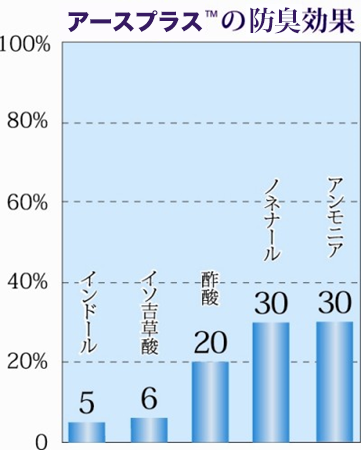
防臭効果は試験開始より2時間後のもの
- 防臭性能試験方法
- 社団法人 繊維評価技術協議会
消臭加工繊維製品認証基準機器分析実施マニュアル
繊維製品抗菌評価法 ISO20743
洗濯回数100回後の抗菌性の確認を実施。
洗濯方法は抗菌加工繊維製品(特定用途)の試験方法(高温加速洗濯法)による。
(洗剤はJAFET標準配合洗剤を使用)
黄色ブドウ球菌 (ATCC6538)
| 基材 | 接種直後 | 18時間後 | 低減率 |
|---|---|---|---|
| アースプラスTM加工布 | 239,000 | <20 | 99.9%以上 |
| 未加工布 | 239,000 | 1,510,000 | – |
肺炎桿菌 (ATCC4352)
| 基材 | 接種直後 | 18時間後 | 低減率 |
|---|---|---|---|
| アースプラスTM加工布 | 10,500 | <20 | 99.9%以上 |
| 未加工布 | 10,500 | 1,750,000 | – |
MRSA (ATCC33592)
| 基材 | 接種直後 | 18時間後 | 低減率 |
|---|---|---|---|
| アースプラスTM加工布 | 368,000 | <20 | 99.9%以上 |
| 未加工布 | 368,000 | 3,760,000 | – |

ホーエンシュタイン研究所から発行された認定タグ
※日本の生菌加工(特定用途医療機関向け)であるSEK赤ラベルの必須菌を対象に行いました。
- 結果
- 洗濯回数100回後の生地においても抗菌性が認められる
- 評価機関
- ドイツ/ホーエンシュタイン研究所
- 試験方法
- DIN EN ISO 20743A,Z:2007-10
- 供試菌
-
黄色ブドウ球菌 Staphylococcus aureus ATCC 6538
肺炎桿菌 Klebsiella pneumoniae ATCC4352
MRSA Staphylococcus aureus(MRSA) ATCC33592
抗菌性評価試験法 ISO22196
MRSA (ATCC33592)
| 基材 | 接種直後 | 18時間後 | 低減率 |
|---|---|---|---|
| アースプラスTM ペイントタイプ |
95,300 | <20 | 99.9%以上 |
大腸菌 (ATCC8739)
| 基材 | 接種直後 | 18時間後 | 低減率 |
|---|---|---|---|
| アースプラスTM ペイントタイプ |
264,000 | 1,622 | 99.3%以上 |

ホーエンシュタイン研究所から発行された認定タグ
- 評価機関
- ドイツ/ホーエンシュタイン研究所
- 試験方法
- ISO 22196:2007-10
- 供試菌
-
MRSA Staphylococcus aureus(MRSA) ATCC33592
大腸菌 Escherichia coli ATCC8739
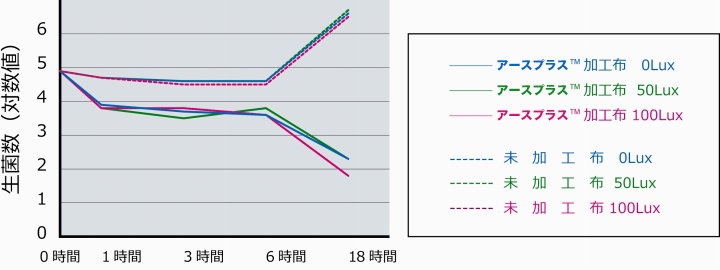
照度と抗菌性能
照度の違いによる抗菌性の確認を実施。
時間経過による「アースプラスTM」と未加工布における生菌数(対数値)の変化を確認した。
- 結果
- 光の強度による抗菌性に顕著な差は認められない。いずれの照度においても抗菌性が認められる
- 使用検体
- アースプラスTM加工布(ペイントタイプ)
- 試験方法
- JIS L 1902
- 供試菌
- 黄色ブドウ球菌 ATCC6538
- 照度計
- DIGITAL LUX METER MODEL:LX-1010B
ダニアレルゲン試験
- 評価機関
- ITEA株式会社 東京環境アレルギー研究所
- 実験名
- ダニアレルゲン(Der f 1)に対する反応実験
- 実験の目的
- アースプラスTM加工不織布について、時間経過に伴うダニアレルゲン濃度を測定する
- 試料
- アースプラスTM加工不織布
- 対照
- 未加工布
- 試料サイズ
- 4×5[cm]
- 実験濃度
- 100[ng/ml]
- 反応条件
-
温度:4[℃]
反応時間:0/6/24[時間]
- 添加量
- 1試料につき各1000[μl]
- アレルゲン溶液
-
ダニアレルゲン(Der f 1)
アレルゲン溶液/ダニ粗抽出物
(設定アレルゲン濃度100ng/ml)
- 実験サンプル数
- 各n=1×3回(日付を独立して実施)
- 測定サンプル
- 試料を反応させたアレルゲン溶液
- 方法
- 試料にダニアレルゲン溶液(ダニアレルゲンを含む)を添加し、反応条件下で放置した。対照は加工していない試料にアレルゲン添加したもののみにした。所定時間経過後、試料を回収してアレルゲン溶液中の濃度を測定した。
- アレルゲン測定
-
酵素免疫測定法(サンドイッチELISA)
96穴マイクロプレートの各ウェルに1次抗体を固相しアレルゲンを補足させた。次に予め標識化した2次抗体を反応させ、酵素、基質を順に反応させた。発色した各ウェルの吸光度を測定し、標準曲線から検体の抗原量を求めた。
ダニアレルゲン(Der f 1)の測定結果
(ng/ml)
| 0h | 6h | 24h | ||
|---|---|---|---|---|
| アースプラスTM加工不織布 | ① | 58.31 | 11.29 | 6.123 |
| ② | 101.53 | 20.15 | 5.3 | |
| ③ | 90.86 | 0.41 | 0.10 | |
| 平均 | 83.57 | 10.62 | 3.84 | |
| 標準偏差 | 22.51 | 9.89 | 3.27 | |
| 未加工布 | ① | 58.31 | 72.74 | 59.1 |
| ② | 101.53 | 118.08 | 115.74 | |
| ③ | 90.86 | 85.94 | 90.81 | |
| 平均 | 83.57 | 92.25 | 88.55 | |
| 標準偏差 | 22.51 | 23.32 | 28.39 | |
時間経過に伴うダニアレルゲン濃度の推移(平均値)
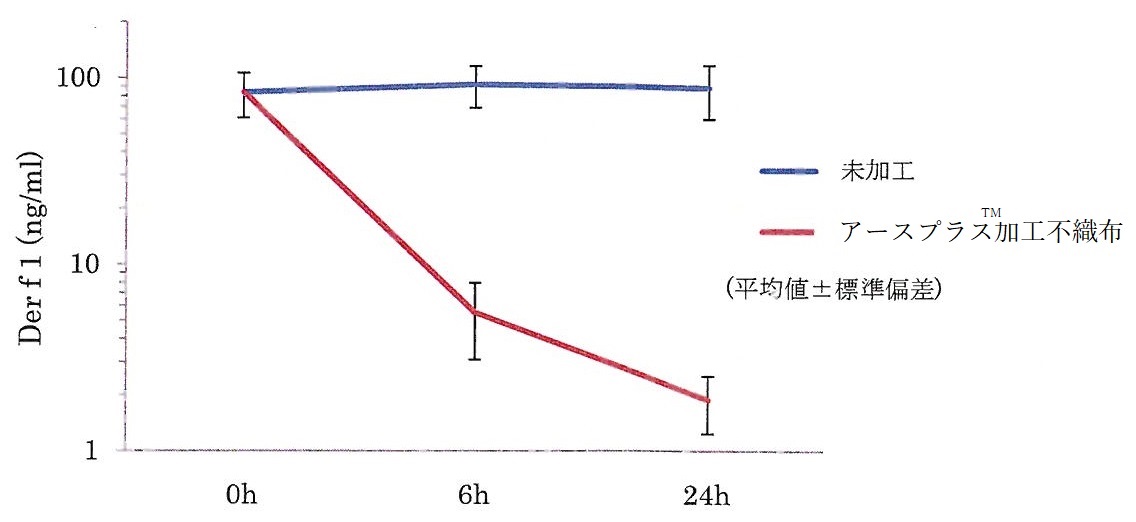
付記
未加工品におけるアレルゲン低減の理由としては、素材における非特異的な吸着、含有成分におけるアレルゲン低減作用等が考えられます。
スギ花粉アレルゲン試験
- 評価機関
- ITEA株式会社 東京環境アレルギー研究所
- 実験名
- アースプラスTM加工不織布とスギ花粉アレルゲンとの反応の検討
- 実験の目的
- アースプラスTM加工不織布について、スギ花粉アレルゲン濃度の低減効果を検討する
- 試料
- アースプラスTM加工不織布
- 対照
- 未加工布
- 試料サイズ
- 2×5[cm]
- 反応条件
-
温度:4[℃]
その他条件:冷蔵庫内の蛍光灯照射下、一晩静置
- 添加量
- 1布片につき各500[μl]
- 対象アレルゲン
- スギ花粉アレルゲン(Cry j 1)
- アレルゲン溶液
-
アレルゲン粗抽出液(Cryj1)
アレルゲン溶液/スギ花粉抽出物
(設定アレルゲン濃度 100ng/ml)
- 実験サンプル数
- 各n=3
- 測定サンプル
- 試料と反応させたアレルゲン溶液を回収し、回収された検体
- 方法
- 試料にアレルゲン溶液を含んだ緩衝液を添加し、試料と接触後の溶液中アレルゲン濃度を測定する
- アレルゲン測定
-
酵素免疫測定法(サンドイッチELISA)
96穴マイクロプレートの各ウェルに1次抗体を固相しアレルゲンを補足させた。次に予め標識化した2次抗体を反応させ、酵素、基質を順に反応させた。発色した各ウェルの吸光度を測定し、標準曲線から検体の抗原量を求めた。
スギ花粉アレルゲン濃度
(ng/ml)
| 0h | 24h | |||
|---|---|---|---|---|
| 測定値 | 平均値 | 標準偏差 | ||
| アースプラスTM加工不織布 | 116.14 | <0.50 | <0.50 | 0 |
| <0.50 | ||||
| <0.50 | ||||
| 未加工布 | 86.09 | 77.44 | 12.93 | |
| 67.80 | ||||
| 78.42 | ||||
スギ花粉アレルゲン濃度の減少効果
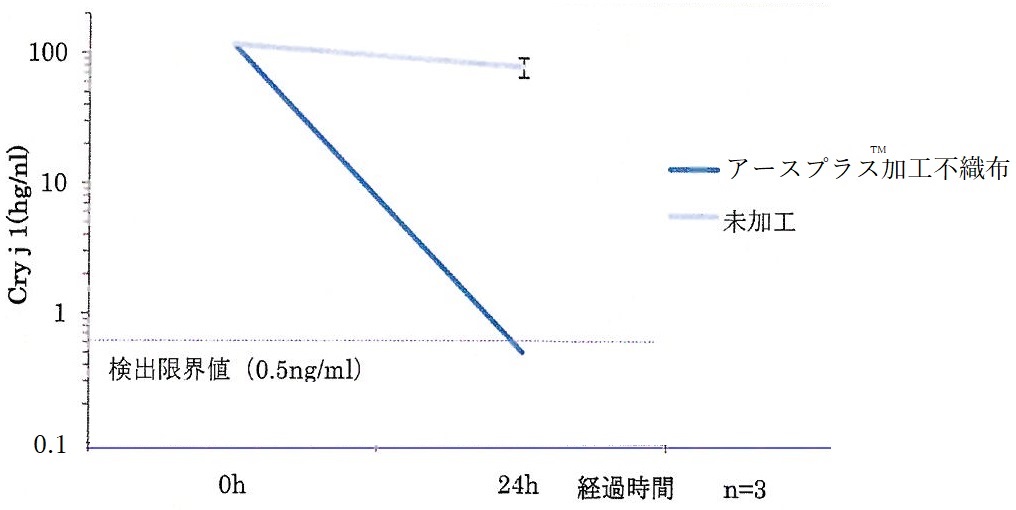
安全性データ
皮膚感作性試験
「アースプラスTM」のモルモットを用いた皮膚感作性試験 (Adjuvant and Patch Test)
- 試験番号
- B020880
- 試験委託者
- 株式会社信州セラミックス
- 試験日
- 2003年1月20日
- 試験責任者
- 株式会社三菱安全科学研究所 毒性研究部 大竹誠司
考察および結論
本試験では「アースプラスTM」の皮膚感作性をAdjuvant and Patch Testにより検討した。
惹起の結果、被験物資投与群および被験物質対象群では、いずれの動物の被験物質投与部位にも皮膚反応は認められなかった。従って、被験物質は本試験条件下で皮膚感作性を示さないと考えられる。
一方、陽性対照群では、全例のDNCB投与部位に明らかな皮膚反応が認められたことから、本試験の実験手順は適切であったと考えられる。
以上のことから、本試験条件下で、「アースプラスTM」はモルモットに対して皮膚感作性を示さないと結論した。
細胞毒性試験
「アースプラスTM」の抽出液を用いた細胞毒性試験(コロニー形成阻害試験)
- 試験番号
- B10757
- 試験委託者
- 株式会社信州セラミックス
- 試験日
- 2003年1月20日
- 試験責任者
- 株式会社三菱安全科学研究所 毒性研究部 大竹誠司
考察および結論
「アースプラスTM」の細胞毒性を、V79細胞を用いたコロニー形成阻害試験により検討した。
コロニー形成試験の結果、被験物質抽出液処理プレートでは、抽出液の濃度に依存して、コロニー形成率が低下し、被験物質は細胞毒性を示すものと考えられた。また被験物質抽出液IC50は53.5%(95%信頼限界:47.3~63.0%)であり、標準材料BのIC50(69.7%)と比較して低値であり、標準材料AのIC50(2.3%)と比較して高値であった。したがって、被験物質の細胞毒性は標準材料Bより強く、標準材料Aより弱いものであると考えられる。
一方、標準材料Aおよび標準材料Bの抽出液IC50は、それぞれ7%未満および70%未満であり、陰性材料抽出液処理プレートと陰性対照プレートの形成数に有意な差は認められなかった。これらの標準材料A,標準材料Bおよび陰性材料を用いた結果は、適用ガイドラインに示された5.5項の条件を満たすものであり、本試験条件は適切なものであったと考えられる。
以上の結果から、「アースプラスTM」はV79細胞に対して細胞毒性を示し、そのIC50は53.5%(95%信頼限界:47.3~63.0%)であると結論した。また、「アースプラスTM」のV79細胞に対する細胞毒性は、標準材料Bより強く、標準材料Aより弱いものであると結論した。
急性毒性試験
「アースプラスTM」のラットを用いた口径投与による急性毒性試験
- 試験番号
- 9L384
- 試験委託者
- 株式会社信州セラミックス
- 試験日
- 1999年8月6日
- 試験責任者
- 株式会社三菱安全科学研究所 石井宏幸
試験目的
「アースプラスTM」をラットに1回口径投与したときの急性毒性を検討する
結果および考察
- 1. 死亡
- 観察期間中、死亡例は認められなかった
- 2. 一般状態
- 観察期間中、異常は認められなかった
- 3. 体重(Table1, 2)
- 観察期間中、順調に増加した
- 4. 剖検所見
- 異常は認められなかった
- 5. 考察
-
「アースプラスTM」の急性口径毒性を検討するため、2000mg/Kgの雄雌のラットに投与した結果、死亡例はみられず、一般状態、体重推移および剖検においても異常は認められなかった。
従って、本試験条件下における「アースプラスTM」の最小致死量(LDLo値)は2000mg/Kg以上であった。
復帰突然変異試験
「アースプラスTM」の細菌を用いる復帰突然変異試験
- 試験番号
- B10756
- 試験委託者
- 株式会社信州セラミックス
- 試験責任者
- 社団法人日本油料検定協会総合分析センター
結果および考察
本試験において、被験物質により誘発された復帰変異コロニー数は、S9mix非共存下および共存下において各テスト菌株の溶射対照値の2倍以上を示さなかった。
この結果は、用量設定試験においても、同様の結果が得られており、再現性が確認された。
- 無菌テストの結果、雑菌の混入は認められなかった
- テスト菌株の生育障害は認められなかった
- プレート上に沈殿析出が認められ、その用量に+印を付した
使用菌株の生菌数は下記のとおりであった。
| 菌株名 | 塩基対置換型 | フレームシフト型 | ||||
|---|---|---|---|---|---|---|
| TA100 | TA1535 | WP2uvrA- | TA98 | TA1537 | ||
| 生菌数 | 用量設定試験 | 3.7 | 3.7 | 5.5 | 3.9 | 2.0 |
| (×109/ml) | 本試験 | 3.8 | 4.3 | 4.7 | 3.9 | 2.6 |
なお、S9 mix非共存下および共存下において陽性対照が各菌株に誘発した復帰変異コロニー数は、各菌株の溶射対照の復帰変異コロニー数と比較して、明らかに2倍を超えて増加し、陽性の結果を示し、また溶射対照値および陽性対照値の平均値は、当総合分析センターの背景データの範囲内であり、試験が適切に実施されたことを示した。
以上の結果から、「アースプラスTM」の変異原性は陰性と結論した。
ヒトパッチテスト
「アースプラスTM」健常人の皮膚に対する刺激性の有無の検討
- 試験委託者
- 株式会社信州セラミックス
- 試験日
- 2002年12月4日
- 試験責任者
- 社団法人日本毛髪科学協会 理事長 渡辺靖
- 1. 試験の目的
- 健常人の皮膚に対する刺激性の有無の検討
- 2. 試料
- 「アースプラスTM」加工生地
- 3. 試験方法
-
被験者:年齢27歳から61歳までの男性12名、女性13名、計25名とした
- 貼付量:10×10mm
- パッチテストの方法:10×10mmの小片をフィンチャンバー(EPITEST Ltd.Oy製造)用のテープを用いて、被験者の上腕屈側部に48時間閉塞貼付けを行い判定した。すなわち貼付後48時間を経過した時点で試料を除去し、除去後1時間及び除去後24時間にそれぞれの皮膚の状態を観察して判定を行った
- 4. 試験の結果
- 被験者25名について行ったパッチテストの結果はすべて陰性であった。そして試料除去後24時間(別表には判定時間72時間として示す。)の反応もすべて陰性で異常は認められなかった。
試験担当者による総評
貴社からの依頼に基づいて実施したパッチテストの結果は上記の通りで、提出された試料〈「アースプラスTM」加工生地〉は刺激反応をおこす可能性の少ない製品と考えられる。
本資料は私が実施した試験結果に基づいて作成されたものに相違ありません。
医師 永島敬士
皮膚一次刺激性試験
「アースプラスTM」ウサギを用いた皮膚一次刺激性試験
- 試験番号
- 第397050222-002号
- 試験委託者
- 株式会社信州セラミックス
- 試験日
- 1999年6月13日
- 試験責任者
- 財団法人日本食品分析センター東京本部
要約
抗菌タオル(「アースプラスTM」塗料化印刷品)を検体として、OECD科学物質毒性試験指針(1981)に準拠し、皮膚一次刺激性試験を行った。
検体のシャーリング面をウサギ3匹の無傷及び有傷皮膚に、4時間閉塞貼り付けした結果、ウサギの皮膚に対する刺激性は認められなかった。
- 1. 試験方法
-
各々の試験動物の体幹背部被毛を試験の24時間前に剃毛した。
体重測定後、試験動物1匹につき、約 6cm2 の面積で4ヶ所を設定し、そのうち2ヶ所には真皮までは達しないように角化層に擦傷を付け(有傷皮膚)、他の2ヶ所を無処置(無傷皮膚)とした。
検体を約 2cm×3cmに裁断し、シャーリング面を約 0.5mlの精製水で湿潤させ、無傷及び有傷皮膚の各1ヶ所ずつに貼り付けした後、絆創膏(日局)で固定した。また、検体が皮膚と接触するように、更に3M-Blenderm手術用テープで保持した。残りの無傷及び有傷は対象とした。曝露時間は4時間とし、その後検体を取り除き、曝露面を精製水で清拭した。除去後、1, 24, 48及び72時間に観察を行い、表-1に従って刺激反応の採点を実施した。
- 2. 試験結果
- 検体除去後の各観察時間において、試験動物 3匹のいずれにも刺激反応は認められなかった。
学術発表
- 2011年 International Journal of Nanomedicine
- 『アースプラスTM(酸化チタン、ハイドロキシアパタイト、銀)加工した綿織布とポリプロピレン不織布に付着する細菌の活動 信州大学医学部と論文発表』
- 2011年 日本感染症学会
-
『セラミックス複合材「e+(アースプラスTM)」による抗菌効果の評価』(繊維)
信州大学医学部とポスター発表
- 2012年 Household and Personal Care Products
- Antibacterial efficacyof TiO2/Ag treated fabricsファブリックの細菌制御目的の抗菌性を基にした二酸化チタン銀(アースプラスTM)アリゾナ大学と論文発表
- 2013年 日本環境感染症学会
- 『継続する新しい殺菌材料「アースプラスTM」による抗ウイルス効果の基礎的な検証』(綿シーツの抗ウイルス性に関して)ポスター発表
- 2014年 Healthcare Infection Society※1
- 『多剤耐性菌※2へのアースプラスTMの抗菌効果』について。東北大学大学院、福島県立医科大学よりポスター発表
※1 Healthcare Infection Societyは、イギリスの感染制御学の学会。医療関連感染に関わる世界で最も権威のある学会の一つと言われている。
※2 多剤耐性菌とは、多くの抗菌薬(抗生剤)が効かなくなった細菌のこと。
お問い合わせはこちら
0264-55-1221
FAX. 0264-55-1181
メールでのお問い合わせ